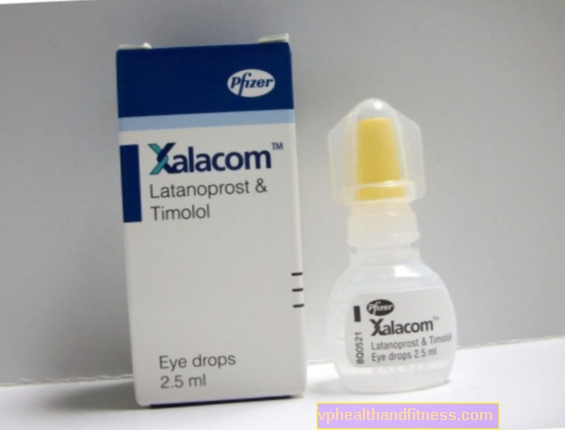
1 ml opløsning indeholder 0,05 mg latanoprost og 5 mg timolol (som maleat). Præparatet indeholder benzalkoniumchlorid.
| Navn | Pakkens indhold | Det aktive stof | Pris 100% | Sidst ændret |
| Xalacom® | sko. 2,5 ml, øjendråber, opløsning. | Latanoprost, Timolol | PLN 40,79 | 2019-04-05 |
Handling
Præparatet indeholder to aktive stoffer, der reducerer det intraokulære tryk som følge af forskellige virkningsmekanismer. De kombinerede virkninger af begge lægemidler resulterer i større reduktioner i IOP end når begge lægemidler blev brugt alene. Latanoprost er en prostaglandin F2a-analog, en selektiv prostanoid FP-receptoragonist. Det sænker det intraokulære tryk ved at øge udstrømningen af vandig humor - øger choroid-scleral flow og reducerer modstanden mod udstrømning gennem det trabekulære net. Det har ingen signifikant effekt på produktionen af vandig humor, den blod-vandige barriere og den intraokulære blodcirkulation. Efter injektion i bindehinden absorberes den gennem hornhinden og hydrolyseres til den biologisk aktive syre af latanoprost. Den maksimale koncentration af lægemidlet i den vandige humor forekommer ca. 2 timer efter administration. T0,5 i plasma er ca. 17 minutter. Efter topisk administration er den systemiske biotilgængelighed af syren i latanoprost 45%. Latanoprost-syre er 87% bundet til plasmaproteiner. Metabolisme finder hovedsageligt sted i leveren. Inaktive metabolitter udskilles hovedsageligt i urinen. Timolol er en ikke-selektiv β-blokker, uden indre sympatomimetisk aktivitet, direkte myokardieinhibering og ikke-specifikke membranstabiliserende virkninger. Timolol reducerer det intraokulære tryk ved at reducere produktionen af vandig humor i det ciliære epitel. Der blev ikke fundet nogen signifikant virkning på permeabiliteten af den blodvandige væskebarriere over for plasmaproteiner. Den maksimale koncentration i den vandige humor forekommer ca. 1 time efter topisk administration af lægemidlet. En del af dosis trænger ind i blodbanen - den maksimale plasmakoncentration nås efter 10-20 minutter. T0,5 i plasma er 6 timer. Metabolisme forekommer i leveren. Timolol-metabolitter udskilles i urinen med uændret lægemiddel. Der er en tendens til en dobbelt så høj koncentration af latanoprost i den vandige humor 1-4 timer efter administration af øjendråber indeholdende latanoprost og timolol sammenlignet med monoterapi.
Dosering
Voksne (inklusive ældre): 1 fald i eller i begge berørte øjne en gang dagligt. Hvis man glemmer en dosis, skal behandlingen fortsættes med den næste planlagte dosis. Hvis der anvendes andre topikale oftalmiske lægemidler, skal der være mindst 5 minutter mellem administrationen. Hvis den nasolakrimale kanal under instillation komprimeres, eller øjenlågene lukkes i 2 minutter, reduceres systemisk absorption. Dette kan begrænse lægemidlets systemiske virkninger og øge dets lokale virkninger.
Indikationer
IOP-reduktion hos patienter med åbenvinklet glaukom og forhøjet IOP hos hvem respons på topiske betablokkere eller prostaglandinanaloger er utilstrækkelig.
Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne. Sygdomme forbundet med bronchial hyperresponsivitet, inklusive astma, historie med bronchial astma og svær kronisk obstruktiv lungesygdom. Sinusbradykardi, syg sinussyndrom, sinoatrisk knudeblok, anden fase atrioventrikulær blok. eller IIIst. ukontrolleret af en pacemaker, åbenlyst hjertesvigt, kardiogent shock.
Forholdsregler
Betablokkeren i timolol absorberes i blodbanen og forårsager bivirkninger, ligesom systemiske betablokkere, herunder dem, der er relateret til det kardiovaskulære og pulmonale system (forekomsten er lavere end for systemisk administration). Patienter med hjerte-kar-sygdomme (fx koronararteriesygdom, Prinzmetals syndrom, hjertesvigt) og hypotension behandlet med betablokkere bør vurderes kritisk, og behandling med andre aktive stoffer bør overvejes. Patienter med hjerte-kar-sygdomme bør overvåges for tegn på forringelse af disse sygdomme eller bivirkninger. På grund af den negative virkning på ledning bør β-blokkere administreres med forsigtighed til patienter med hjerteblok Ist. Hos patienter med alvorlige perifere kredsløbssygdomme (f.eks. Alvorlige former for Raynauds sygdom eller Raynauds syndrom) skal passende forholdsregler tages. Åndedrætssymptomer, inklusive død fra pludselig bronkospasme hos patienter med astma, er rapporteret efter okulær administration af nogle betablokkere. Det bør anvendes med forsigtighed til patienter med mild og / eller moderat kronisk obstruktiv lungesygdom (KOL) og kun hvis fordelene opvejer de potentielle risici. Betablokkere bør anvendes med forsigtighed til patienter med risiko for spontan hypoglykæmi eller hos diabetespatienter (især dem med utilstrækkelig kontrolleret diabetes), da de kan maskere tegn og symptomer på akut hypoglykæmi. Betablokkere kan også maskere symptomerne på en overaktiv skjoldbruskkirtel. Pludselig seponering af behandlingen kan gøre din sygdom værre. Oftalmiske betablokkere kan forårsage tørhed i øjnene - patienter med hornhindesygdomme bør behandles med forsigtighed.Hos patienter, der modtager samtidig systemiske β-blokkere, kan der forekomme en stigning i den IOP-sænkende virkning eller kendte virkninger af systemisk β-adrenerg blokade med timolol. Sådanne patienter bør overvåges nøje. Under anvendelse af betablokkere kan patienter med en historie med atopisk sygdom eller en historie med alvorlige anafylaktiske reaktioner på forskellige allergener være mere følsomme over for geneksponering for allergener og reagerer muligvis ikke på de sædvanlige doser af adrenalin, der anvendes til behandling af anafylaktiske reaktioner. Koroid frigørelse efter filtreringsprocedurer er blevet observeret ved brug af lægemidler, der reducerer det intraokulære tryk (f.eks. Timolol, acetazolamid). Oftalmiske betablokkere kan blokere de systemiske virkninger af beta-agonister, såsom for eksempel adrenalin. Anæstesilægen skal informeres, når patienten får timolol. En gradvis tilbagetrækning af β-blokkere inden større operationer bør overvejes. Betablokkere forstyrrer hjertets evne til at reagere på beta-adrenerg stimulering, hvilket kan øge risikoen for generel anæstesi under operationen. Der har været rapporter om langvarig svær hypotension under anæstesi og vanskeligheder med at genstarte og opretholde hjertefrekvensen. Under operationen kan virkningerne af β-adrenerge blokkere vendes ved administration af passende doser af adrenerge agonister. Brug af to lokale betablokkere eller to lokale prostaglandiner anbefales ikke. Latanoprost kan gradvist ændre øjenfarve ved at øge mængden af brunt pigment i iris. Ændringen i irisens farve er ikke forbundet med nogen bivirkninger eller patologiske ændringer. Patienter bør dog overvåges regelmæssigt, og seponering af behandlingen kan overvejes, hvis der er en stigning i irispigmentering og afhængigt af den kliniske tilstand. I øjeblikket er der ingen erfaring med brugen af latanoprost til: inflammatorisk, neovaskulær glaukom, kronisk lukketvinklet glaukom, åbenvinklet glaukom hos patienter med pseudophakia og pigmentær glaukom. Latanoprost har ringe eller ingen effekt på pupillerne og er endnu ikke brugt til akutte angreb af vinkellukningsglaukom. Der skal udvises forsigtighed ved administration af lægemidlet i disse sygdomstilstande, indtil komplette data er tilgængelige. Latanoprost bør anvendes med forsigtighed til patienter med historie med herpetisk keratitis. Undgå brug hos patienter med nuværende herpetisk keratitis og hos patienter med en historie med tilbagevendende herpetisk keratitis forbundet med prostaglandinanalog brug. Makulaødem, inklusive dets cystiske form, er rapporteret ved behandling med latanoprost, hovedsageligt hos afakiske, pseudofakiske patienter med revet bageste linsekapsel og også hos patienter med risiko for makulaødem. Præparatet skal anvendes med forsigtighed hos disse patienter. Forøget muskelsvaghed forårsaget af timololmaleat (fx diplopi, ptosis, generaliseret svaghed) er rapporteret hos nogle patienter med myasthenia gravis eller med symptomer på myasthenia gravis. Præparatet indeholder benzalkoniumchlorid, som kan forårsage punktat keratitis og / eller toksisk ulcerøs keratitis eller øjenirritation og ændre farven på bløde kontaktlinser. Hos patienter med tør øjensyndrom og hos patienter med hornhindelæsioner kræver hyppig eller langvarig anvendelse af præparatet nøje overvågning. Benzalkoniumchlorid kan absorberes af kontaktlinser og bør fjernes inden administration. Linser kan påføres igen 15 minutter efter indgivelse af dråberne. Sikkerheden og effekten af præparatet hos børn og unge er ikke fastslået.
Uønsket aktivitet
Meget almindelig: Øget pigmentering af iris (især hos patienter med blandet iris, f.eks. Grønbrun, gulbrun eller blå / gråbrun; farveændringen på iris er meget langsom, det er ikke forbundet med nogen bivirkninger eller patologiske ændringer) , kan det være permanent; hos patienter med homogene blå, grå, grønne eller brune øjne forekommer misfarvningen kun i isolerede tilfælde). Almindelig: diabetes mellitus, hyperkolesterolæmi, depression, hovedpine, øjenirritation (inklusive stikkende, brændende og kløende fornemmelser), øjensmerter, øjenirritation (herunder stikkende, brændende og kløende fornemmelse), øjensmerter, unormal syn, blefaritis, sygdom konjunktivitis, konjunktivitis, øjenrødme, keratitis, hornhindesygdom, fotofobi, hirsutisme og hudlidelser, epitelpletter, tørre øjne, hævelse af øjenlåg. Ikke almindelig: sløret syn, øget lakrimation, hududslæt, kløe. Yderligere bivirkninger forbundet med brugen af individuelle komponenter i præparatet. Latanoprost: meget almindelig: ændringer i vipperne og det originale hår (øget længde, tykkelse, pigmentering og mængde); almindelig: punkterede epiteldefekter, tørre øjne, øjenlågsødem; ikke almindelig: ustabil angina, brystsmerter; Ikke kendt: herpetisk keratitis, svimmelhed, iritis og / eller uveitis, makulaødem inklusive cystisk makulaødem, forkert styrede øjenvipper, som undertiden fører til øjenirritation, hævelse af hornhinden og erosioner, dobbelt rækkeudseende øjenvipper på skjoldbruskkirtlenes åbninger (distichiasis), ændringer i øjenhulerne og øjenlågene, hvilket resulterer i uddybning af øjenlågens fure, iriscyste, hjertebanken, astma, astmaforværring, åndenød, mørkhed af øjenlågets hud, hudreaktioner på øjenlågene, muskelsmerter, ledsmerter. Timolol: hyppighed ikke kendt: systemisk allergisk reaktion, inklusive angioødem, urticaria, anafylaktisk reaktion, hypoglykæmi, maskering af symptomer på hypoglykæmi, søvnløshed, mareridt, hukommelsestab, adfærdsændringer og mentale lidelser, herunder følelse af forvirring, hallucinationer, rastløshed, forvirring, nervøsitet, besvimelse, slagtilfælde, cerebral iskæmi, forværring af myasthenia gravis, paræstesi, tegn og symptomer på øjenirritation (fx brændende, stikkende, kløe, tåreflåd, rødme), koroideafløsning efter filteroperation, nedsat hornhindefornemmelse, hornhindeerosion , ptose, diplopi, tinnitus, bradykardi, ødem, arytmier, kongestiv hjertesvigt, atrioventrikulær blok, hjertestop, hjertesvigt, nedsat blodtryk, Raynauds fænomen, kolde hænder og fødder symptom, bronkospasme (hovedsagelig hos patienter med et tidligere udseende bronkospasme), dyspnø, hoste, nasal obstruktion, lungeødem, åndedrætsbesvær, dysgeusi, kvalme, fordøjelsesbesvær, diarré, mundtørhed, mavesmerter, opkastning, retroperitoneal fibrose, alopeci, pseudopemfigoid, psoriasislignende udslæt eller forværring symptomer på psoriasis, seksuel dysfunktion, nedsat libido, træthed. Hos nogle patienter med alvorligt beskadigede hornhinder er der rapporteret om meget sjældne tilfælde af forkalkning af hornhinden i forbindelse med anvendelse af fosfatholdige øjendråber.
Graviditet og amning
Præparatet bør ikke anvendes under graviditet og amning.
Kommentarer
Inden behandlingen påbegyndes, bør patienterne informeres om muligheden for misfarvning af iris i det behandlede øje. Behandling af det ene øje kan føre til permanent heterokromi. Du kan opleve en midlertidig periode med sløret syn, når du bruger øjendråber - indtil dette er forsvundet, må du ikke føre motorkøretøj eller betjene maskiner.
Interaktioner
Der er rapporteret om paradoksale stigninger i intraokulært tryk efter samtidig administration af to prostaglandinanaloger til øjet. Derfor anbefales ikke anvendelse af to eller flere prostaglandiner, prostaglandinanaloger eller prostaglandinderivater. Det er muligt at intensivere præparatets virkning og inducere hypotension og / eller signifikant bradykardi, når der anvendes øjendråber med en beta-blokker med orale calciumkanalblokkere, betablokkere, antiarytmika (inklusive amiodaron), digitalisglykosider, parasympatomimetika udskylning af catecholaminer og guanethidin. Tilfælde af systemisk forstærkning af β-blokade (fx nedsat hjertefrekvens, sammenbrud) er rapporteret, når timolol administreres sammen med CYP2D6-hæmmere (fx quinidin, fluoxetin, paroxetin). Virkningen på det intraokulære tryk eller den kendte effekt på systemisk β-blokade kan øges, når præparatet anvendes til patienter, der får orale β-blokkere, og det anbefales derfor ikke at anvende to eller flere β-blokkere topisk. Mydriasis er lejlighedsvis rapporteret under samtidig administration af oftalmiske betablokkere med adrenalin (adrenalin). Forhøjelsen af blodtrykket efter pludselig tilbagetrækning af clonidin kan forstærkes med betablokkere. Betablokkere kan øge den hypoglykæmiske virkning af antidiabetika. De kan maskere tegn og symptomer på hypoglykæmi.
Pris
Xalacom®, pris 100% PLN 40,79
Præparatet indeholder stoffet: Latanoprost, Timolol
Refunderet lægemiddel: JA